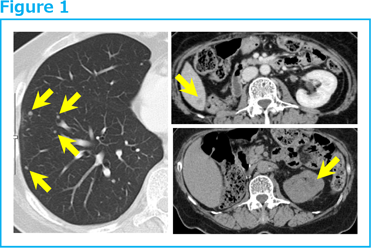
臨床症例報告No.46 (PDF版はこちら) ペムブロリズマブが無効であったが、免疫細胞療法(アルファ・ベータT細胞療法)単独治療により寛解した肺、肝転移を伴う腎盂がん症例
- 種類:腎盂
INTRODUCTION
遺伝性大腸がんの1つであるリンチ症候群では大腸がん以外に卵巣がん、子宮体がん、胃がんなど様々ながんの発症リスクが高まる。リンチ症候群ではMLH1、MSH2などのミスマッチ修復(MMR)遺伝子の変異を伴うことが多く、MMRの機能低下はマイクロサテライト不安定性(MSI)を生じる。MSI-highのがん細胞においては多くの遺伝子変異を持つこととなり、T細胞の認識を受け、免疫系の標的となりやすく、免疫チェックポイント阻害剤(ICI)の有効性が高い。MSI-highの233例の大腸以外の様々な固形がん患者におけるペムブロリズマブ単独治療の奏効率(ORR)は34.3%、無増悪期間は4.1ヶ月、生存期間中央値は23.5ヶ月と報告されている[1]。
腫瘍細胞に対する免疫応答のメカニズムから、免疫細胞治療とICI併用治療の有効性が期待され、われわれは安全性および有効性をみる臨床研究を2017年より行っている。安全性の試験において、低容量のニボルマブと免疫細胞治療の併用で重篤な副作用の発生はなく、また、寛解例も観察された[2]。今回、ICI抵抗性のがんに対して、ICI治療後、免疫細胞治療(アルファ・ベータT細胞療法)を単独で行ったところ著効した症例を経験したので報告し、低容量のICIと免疫細胞治療の併用治療について考察する。
CASE
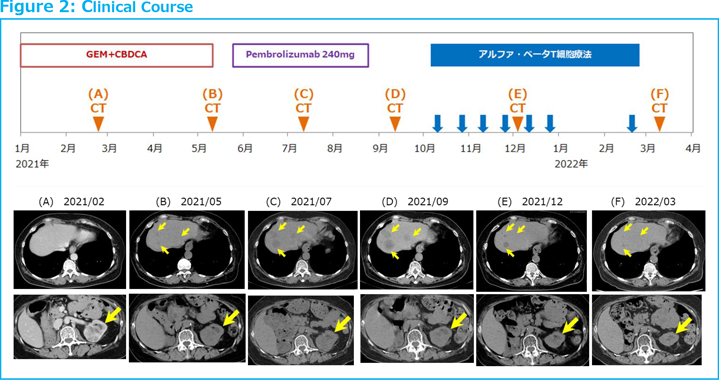
RESULT
DISCUSSION
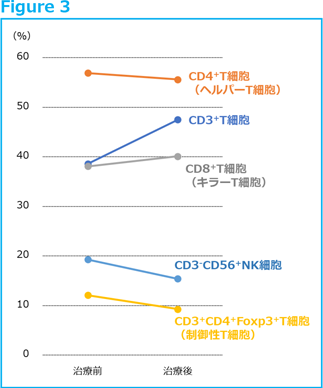
化学療法およびペムブロリズマブ無効の腎盂がんに対して、免疫細胞治療(アルファ・ベータT細胞療法)による寛解例を報告した。T細胞系の減少、アンバランスが診断されたためアルファ・ベータT細胞療法を開始、4回施行後、リンパ球数は著増し、CT画像にて寛解を観察した。4回のアルファ・ベータT細胞療法のみで急速に寛解するケースは少いことから、前治療のペムブロリズマブの影響についても検討したい。0.3から10mg/kgのニボルマブを投与した臨床研究において、いずれの投与量においても、ニボルマブによるT細胞上のPD-1占有率が70%を超えた状態が2ヶ月以上維持されたことが報告されている[4]。また、ペムブロリズマブの半減期は18.4日から27.3日とされている[5、6]。本ケースではアルファ・ベータT細胞療法の51日前まで通常量(240mg)のキイトルーダによる治療が施行されていた。51日後は約1/8~1/4の量、すなわち、40mg~60mgのペムブロリズマブ投与を受けた場合と同様の濃度で体内に残存していたと推測される。すなわち、低容量のICI併用アルファ・ベータT細胞療法と同様の効果が得られた可能性がある。すなわち、ペムブロリズマブ単独治療は無効なるも、アルファ・ベータT細胞療法と低容量のペムブロリズマブの併用治療が奏効したと考えることができる。アルファ・ベータT細胞療法によりリンパ球数の増加およびT細胞率の増加、制御性T細胞率の減少も生じ、抗腫瘍免疫系の改善がペムブロリズマブの効果に繋がったかもしれない。
現状、ニボルマブ、ペムブロリズマブなどの免疫チェックポイント阻害剤が無効であった例では、さらに免疫細胞治療などの免疫療法は行われることはほとんどない。本症例のように、免疫チェックポイント阻害剤無効であった場合でも、その後の免疫細胞治療により著効する場合があることが示唆される。今後の臨床研究により、十分に検証をしていきたい
REFERENCES
- Aurelien M et al: Efficacy of Pembrolizumab in Patients With Noncolorectal High Microsatellite Instability/Mismatch Repair-Deficient Cancer: Results From the Phase II KEYNOTE-158 Study. J Clin Oncol. 1;38(1):1-10, 2020
- Takimoto R. et al. Esophageal cancer responsive to the combination of immune cell therapy and low-dose nivolumab: two case reports. . J Med Case Reports. 15:191, 2021
- Noguchi A, et al. Impaired and imbalanced cellular immunological status assessed in advanced cancer patients and restoration of the T cell immune status by adoptive T-cell immunotherapy. International Immunopharmacology, 18: 90-97, 2014
- Brahmer JR: Phase I study of single-agent anti-programmed death-1 (MDX-1106) in refractory solid tumors: safety, clinical activity, pharmacodynamics, and immunologic correlates. J Clin Oncol.; 28: 3167-3175, 2010
- ペムブロリズマブ(遺伝子組換え) 注射剤 2.5
臨床に関する概括評価https://www.pmda.go.jp/drugs/2016/P20161025002/170050000_22800AMX00696000_G100_1.pdf - 医薬品インタビューフォーム キイトルーダ®点滴静注